Последние конференции
- Информационные системы и модели в научных исследованиях, промышленности, образовании и экологии
- Информационные системы и модели в научных исследованиях, промышленности и экологии
- Современные проблемы экологии
- Экологические проблемы окружающей среды, пути и методы их решения
- Экология, образование и здоровый образ жизни
Исследование увеличения глубины когерентного зондирования в оптической когерентной томографии
К.И.С. Галеб, А.Ю. Потлов, С.Г. Проскурин
Тамбовский государственный технический университет,
г. Тамбов
Оптическая когерентная томография (ОКТ) возникла в конце восьмидесятых, в начале девяностых годов двадцатого века [1]. В начале этого столетия она заняла прочное место в ряду медицинской диагностической техники. ОКТ использует отражённый оптический сигнал от поверхностей различной оптической плотности, и во многом аналогична ультразвуковой (УЗИ) диагностике. Глубина зондирования систем ОКТ составляет 1-2 мм, что существенно меньше чем у систем УЗИ [2] и рентгеновских приборов [3]. Из-за сильного рассеяния оптического излучения в биотканях, ОКТ системы преимущественно применяются для исследования роговицы, стекловидного тела и сетчатки глаза. Однако, разрешение таких систем ОКТ на один, два порядка превышает разрешение систем УЗИ для аналогичных исследований, которое составляет 1 мм – 100 мкм [2].
ОКТ использует принципы сканирующий низкокогерентной интерферометрии (интерферометр Майкельсона). Низкая когерентность непрерывного источника излучения фемтосекундного лазера или суперлюминисцентного диода (СЛД), обеспечивается широкой спектральной полосой, Δλ, что даёт высокое пространственное разрешение в зондирующем плече по глубине сканирования, ?z ~ 0,44 ?2/??.
Локализация продольной компоненты измерительного объёма при использовании СЛД с длиной волны ? = 800-1700 нм, и ?? = 20-100 нм, достигает ?z ~ 5-15 микрон [1, 4]. Такой короткий когерентный пакет соответствует 15-50 фс импульсного лазера. В приложении к сильно рассеивающим тканям кожи человека и животных стандартные ОКТ методы дают возможность визуализации поверхностных слоёв с указанным разрешением на глубину когерентного зондирования (ГКЗ) 1-1,2 мм.
Материалы и методы
В экспериментальной установке (Рис. 1) был использован сканирующий интерферометр Майкельсона выполненный на базе оптических световодов. Излучение СЛД (?=1298 нм, ??=52 нм) поступает в разветвитель световодов 50х50 %, FS1, и далее на второй разветвитель световодов 50х50 %, FS2. Из последнего половина излучения поступает в опорное плечо интерферометра,другая половина поступает в плечо образца и фокусируется на образце при помощи системы линз. Отражённое от обоих плеч интерферометра излучение смешивается на балансных квадратичных фотоприёмниках D1 и D2. После балансной схемы, электрический сигнал поступает на полосовой фильтр, после него на спектроанализатор и на аналого-цифровой преобразователь (АЦП).
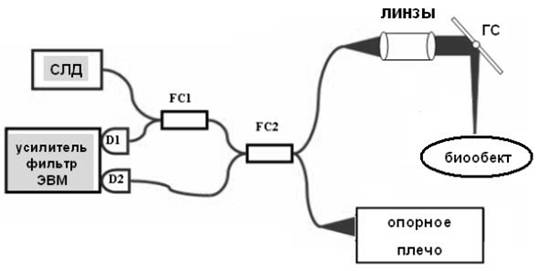
Рис. 1. Схема ОКТ. СЛД – суперлюминисцентный диод; FS1, FS2 – 1х2 и 2х2 разветвители световодов, в опорном плече находится сканирующая оптическая линия задержки, ГС – гальвано-сканер, D1,D2 – инфракрасные детекторы, включённые в балансную схему
После АЦП цифровой сигнал записывается и обрабатывается на компьютере в пакетах LabVIEW и MATLAB. В работах [5, 6] впервые удалось построить быстро сканирующую оптическую линию задержки (ОЛЗ) таким образом, чтобы использовать несущую частоту в пределах 50-100 кГц. В спектральной области это позволяет одновременно отстроиться от низкочастотного 1/f шума и не уводить несущую частоту быстро сканирующей оптической линии задержки в нарастающий белый шум. Усовершенствованная линия задержки позволяет использовать обе длины волны (1,3 и 1,5 мкм) одновременно. В плече образца применяется растровое сканирование и усреднение по нескольким линиям, что увеличивает соотношение сигнал/шум (С/Ш) на 10-15 dB, увеличивает контраст на 20-30 %, и увеличивает ГКЗ на 20-40 %.
Результаты и обсуждение
Описанным методом впервые удалось получить изображение подкожных кровеносных сосудов диаметром ~ 0,2-1 мм около тройника кровеносных сосудов на глубине ~ 1-1,8 мм (Рис. 2). Частота сканирования в плече образца уменьшается, что пропорционально увеличивает время регистрации сигнала, но значительно уменьшает спекл шумы, и увеличивает контраст изображения за счёт увеличения соотношения С/Ш. Более глубокие слои кожи возможно визуализировать только за счёт переходного квазидиффузионного когерентного режима регистрации фотонов. Ухудшение разрешения нижних слоёв в 3-5 раз по сравнению с верхними слоями соответствует наличию рассеяния излучения и перехода в промежуточный режим между когерентной и диффузионной томографией [7]. Это режим слабо рассеянных фотонов всё ещё сохраняющих когерентность с опорным плечом интерферометра.

Рис. 2. ОКТ изображения кожи и подкожных кровеносных сосудов пальца человека около тройника in vivo. Длина волны СЛД ~1.3 мкм
Заключение
В данной работе было использовано дистанционное растровое сканирование, аналогичное сканированию оптических радаров, с последующим усреднением соседних интерферограмм. Описанный подход важен с практической точки зрения. Применённое растровое усреднение в пределах одного А-скана увеличивает соотношение С/Ш на 10-15 dB. При таком соотношении удалось зарегистрировать фотоны в переходном режиме от отражения и обратного рассеяние, к диффузионному режиму многократного рассеяния. Динамически изменяя когерентность источника излучения и несущую частоту сканирования, предполагается добиться соответствия когерентного пакета пространственному разрешению в глубоких слоях биообъекта.
Список литературы
1. Зимняков Д.А., Тучин В.В. Оптическая томография тканей // Квантовая электроника. 2002. Том. 32 (10). С.849-867.
2. Fisher YL, Nogueira F, Salles D. Diagnostic ophthalmic ultrasonography // Duane's Foundations of Clinical Ophthalmology Philadelphia, 2009: chap 108.
3. Abahussin M, Hayes S, at. al. 3D collagen orientation study of the human cornea using X-ray diffraction and femtosecond laser technology // Invest Ophthalmol Vis Sci. 2009. Vol. 50 (11). p. 5159-64.
4. Proskurin S.G., Sokolova I.A., Wang R.K. Imaging of non-parabolic velocity profiles in converging flow with optical coherence tomography // Physics in Medicine and Biology. – 2003. – p. 2907-2918.
5. Proskurin S.G. Comparison of high and low coherence Doppler spectra for human subcutaneous blood flow diagnostics in vivo // Proc. SPIE 5702,2005. - P. 44-53.
6. Proskurin S.G.,Meglinski I.V.Optical coherence tomography imaging depth enhancement by superficial skin optical clearing // Laser Physics Letters. 2007. Vol.4 (11). p. 824-826.
7. Проскурин С.Г., Использование поздно пришедших фотонов для диффузионной оптической томографии биологических объектов // Квант. электроника, 2011. Том. 41 (5), с.402–406.